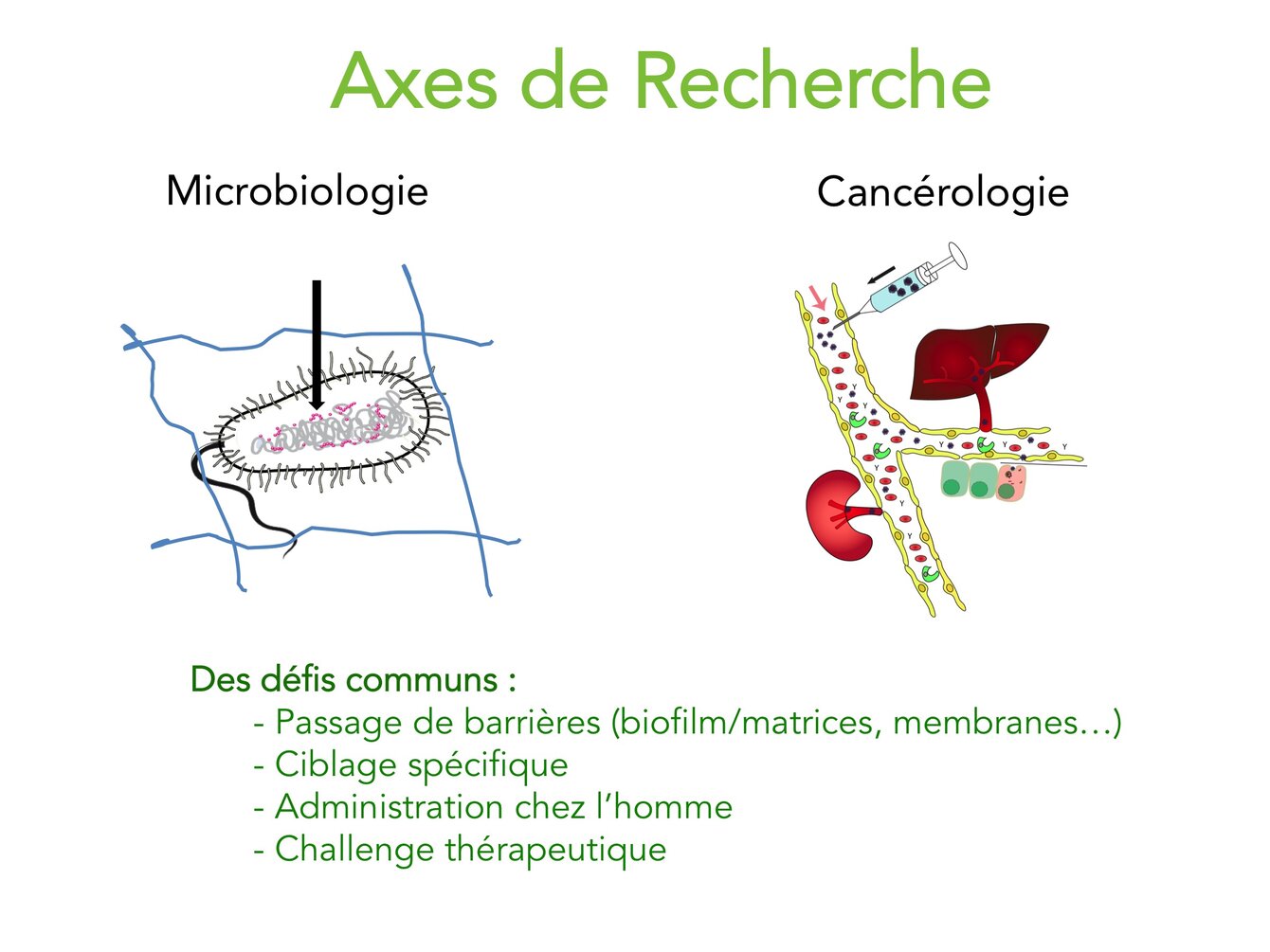
Axe 1: Comment lutter contre l'antibio-résistance des bactéries pathogènes critiques?
Les bactéries s'adaptent facilement aux modifications de leur environnement et développent des stratégies pour résister aux nouveaux traitements antibiotiques. Il est donc nécessaire de continuer à chercher de nouvelles molécules et stratégies pour contrecarrer leur adaptation à l’effet des antibiotiques. Découvrir un nouvel antibiotique est clairement un défi, car chez les bactéries Gram-négatives, l’enveloppe bactérienne constitue un rempart contre les composés bactério-toxiques et, de plus, de nombreuses bactéries pérennisent l’infection en adoptant un mode de croissance sous la forme de biofilms, très imperméables aux agents antibactériens. Dans ce contexte, InnoVec a pour but de mieux comprendre comment les bactéries Gram-négatives passent malgré tout des éléments nutritifs aux travers de ce rempart et propose de développer une palette de stratégies et outils qui favoriseraient l'accès d’antibiotiques à leurs cibles.
Pour y arriver, les équipes d'InnoVec développent des recherches fondamentales pour :
- Comprendre les mécanismes par lesquels les bactéries assurent l'entrée active des nutriments par des systèmes de transport transmembranaires dédiés. Ces « portes d'entrée » peuvent être mises à profit pour le transport sélectif de composés antibactériens (stratégie dite du cheval de Troie).
- Inventer et synthétiser de nouvelles molécules ou dispositifs nanométriques pour favoriser l'accumulation des composés actifs dans les bactéries, au plus près de la cible biologique.
- Concevoir, optimiser et appliquer des dispositifs microfluidiques, des algorithmes mathématiques, de l’intelligence artificielle (AI), pour la mise au point, l’évaluation et l’optimisation des molécules vectorisées.
Axe 2: Comment améliorer la délivrance d'actifs thérapeutiques aux cellules cancéreuses dans leur microenvironnement spécifique ?
Les anticorps monoclonaux dérivés de la biotechnologie ainsi que d'autres substances anti-tumorales chimiques ont permis d'améliorer considérablement le traitement de certains cancers, mais il reste néanmoins des cancers pour lesquels aucun progrès significatif n'est observé. Les raisons des échecs thérapeutiques sont nombreuses et complexes, les cellules tumorales pouvant s'adapter aux traitements en mettant à profit le caractère hétérogène des tumeurs et de leur environnement. Les équipes d'Innovec développent des recherches pour améliorer la délivrance de molécules et le ciblage les cellules tumorales:
- Concevoir des technologies pour favoriser la délivrance d'acides nucléiques et de protéines dans les cellules cancéreuses, qui reposent sur la conception de dérivés d'anticorps, de particules virales, d'assemblages chimiques supramoléculaires et sur l'utilisation de méthodologies électroniques/physiques.
- Développer des stratégies innovantes et les adapter aux systèmes de délivrance pour cibler spécifiquement les voies de signalisation impliquées dans l'agressivité des tumeurs.
- Comprendre comment certaines cellules cancéreuses répondent aux traitements et modifient leurs signatures transcriptomique, épigénétique et protéomique de manière dynamique notamment à l'aide de l'intelligence artificielle (IA) et de la bio-informatique. Ces connaissances permettront d’identifier, à la fois, des cibles membranaires pouvant servir de marqueurs ou de portes d’entrée pour la vectorisation ciblée des cellules cancéreuses, et des cibles intracellulaires actionnables et cruciales pour la survie des cellules cancéreuses.
- Intégrer des biocapteurs dans des laboratoires sur puces ou des systèmes télémétriques, concevoir des algorithmes mathématiques et de l’IA pour mieux comprendre les mécanismes en jeu dans les différentes étapes de la vectorisation d'un principe actif.
- Développer des modèles pertinents reflétant au mieux la réalité clinique pour la validation de preuves de concept de vectorisation/délivrance et favoriser ainsi la translation des résultats vers la clinique.